0708. tbl. 110. árg. 2024
Fræðigrein
Arfgengi smáæðasjúkdómurinn CADASIL
– yfirlitsgrein
doi: 10.17992/lbl.2024.0708.801
Ágrip
CADASIL er skammstöfun á Cerebral Autosomal Dominant Arteriopathy with Subcortical Infarcts and Leukoencephalopathy.
CADASIL tilheyrir hópi arfgengra smáæðasjúkdóma í heila og stafar af sjúkdómsvaldandi stökkbreytingu í NOTCH3-geninu á litningi 19, sem erfist á ríkjandi hátt. Gallaða NOTCH3-próteinið safnast fyrir á yfirborði sléttra vöðvafrumna í litlum slagæðum heilans. Þetta veldur smám saman tapi á sléttvöðvalaginu og örvefsmyndun, æðaveggir í slagæðum verða stífari og þykkari sem leiðir til súrefnisskorts, vefjaskaða og smáæðadreps í hvíta og djúpa gráa efni heilans.
Segulómskoðun sýnir útbreiddar, samhverfar hvítaefnisbreytingar, dæmigert er að breytingarnar komi fram í fremri hluta gagnaugarblaðs og gráhýði. Mígreni með áru, skammvinn heilablóðþurrð eða heilaslag, auk geðrænna einkenna og snemmkominnar heilabilunar eru helstu afleiðingar sjúkdómsins.
Greinin barst til blaðsins 1. maí 2024, samþykkt til birtingar 21. júní 2024.
Inngangur
Nafnið CADASIL er skammstöfun á Cerebral Autosomal Dominant Arteriopathy with Subcortical Infarcts and Leukoencephalopathy.
CADASIL tilheyrir hópi arfgengra smáæðasjúkdóma í heila.1 Sjúkdómnum var fyrst lýst árið 1955 af belgíska taugalækninum Ludo van Bogaert.2 Finnsku vísindamennirnir Vesa Sonninen og Marja-Liisa Savontaus greindu fyrst frá sjúkdóminum á Norðurlöndum.3 CADASIL stafar af sjúkdómsvaldandi stökkbreytingu í NOTCH3-geninu á litningi 19.4 Gallaða NOTCH3-próteinið safnast fyrir á yfirborði sléttra vöðvafrumna í litlum slagæðum heilans.4 Æðaveggir slagæða tapa sléttum vöðvafrumum sem skipt er út fyrir örvef. Fyrir vikið verða æðarnar stífari og þrengri og geta til æðavíkkunar skerðist.5
Mígreni með áru, skammvinn heilablóðþurrð (TIA) eða heilaslag (stroke), auk geðrænna einkenna og snemmkominnar heilabilunar, eru helstu afleiðingar sjúkdómsins. CADASIL er mikilvæg orsök heilaslags og snemmkominnar heilabilunar hjá ungu og miðaldra fólki og líklega vangreint.4
Faraldsfræði
Algengi CADASIL í erlendum rannsóknum er um 2-4 einstaklingar á hverja 100.000 íbúa. Því gætu 8-16 manns verið með sjúkdóminn á Íslandi.6 Faraldsfræði CADASIL á Íslandi hefur ekki verið rannsökuð.
Þar sem einkenni eru oft væg í CADASIL, geta útbreiddar hvítaefnisbreytingar verið ranglega túlkaðar sem aldurstengdar eða orsakaðar af áhættuþáttum smáæðasjúkdóma í heila. Sjúkdómurinn er því líklegast vangreindur. Nýlegar rannsóknir sýna að allt að einn af hverjum 300 beri meinvaldandi stökkbreytingu í NOTCH3-geninu.7 Ekki er ávallt um fulla sýnd (penetrance) að ræða og sjúklingum með vægari sjúkdómsmynd hefur verið lýst.8
Orsök
CADASIL stafar af sjúkdómsvaldandi stökkbreytingu í NOTCH3-geninu á litningi 19 (19p13.12).4 Yfir 200 mismunandi meinvaldandi stökkbreytingar hafa verið greindar. Genið kóðar fyrir NOTCH3-próteininu, en NOTCH innanfrumuboðferlið gegnir mikilvægu hlutverki í tilurð og sérhæfingu alls æðakerfisins.9 NOTCH3 er sérlega mikilvægt í þroska og virkni sléttvöðvalags lítilla og meðalstórra æða heilans (100-400 mikrón í þvermál) og hefur með því áhrif á samdrátt í æðunum og stjórnun á blóðflæði, ekki síst í hvítaefni heilans.10
Sjúkdómsvaldandi stökkbreytingin hefur í för með sér breytingu á byggingu NOTCH3-próteinsins, en afbrigðilega NOTCH3-próteinið myndar skaðlegt fínkorna efni (GOM, granular osmiophilic material) sem hleðst upp á grunnhimnu sléttra vöðvafrumna. Breytingarnar koma fram bæði í sléttvöðvalaginu og æðagrannfrumum (pericytes). Þetta veldur smám saman tapi á sléttvöðvalaginu og örvefsmyndun, æðaveggir í slagæðum verða stífari og þykkari,11 sem leiðir til súrefnisskorts, vefjaskaða og smáæðadreps (lacunar infarction) í hvíta og djúpa gráa efni (basal ganglia) heilans. Heilabörkurinn verður sjaldnar fyrir áhrifum í CADASIL.4
Erfðir
CADASIL erfist á ríkjandi hátt.12 Þetta þýðir að ef annað foreldrið er með sjúkdóminn, eru 50% líkur á því að afkvæmi fái hann. Þau börn sem ekki hafa fengið sjúkdómsvaldandi afbrigði gensins fá ekki sjúkdóminn og bera hann heldur ekki áfram.
CADASIL getur einnig komið upp í kjölfar nýrrar stökkbreytingar. Breytingin hefur þá yfirleitt orðið í einhverri kynfrumu foreldra. Líkur á að foreldrar eignist aftur barn með sjúkdóminn eru innan við 1%. Hins vegar verður nýja afbrigðið í barninu arfgengt og getur þannig borist til næstu kynslóðar í samræmi við ríkjandi erfðamynstur.
Töluverður breytileiki er á því hvenær fólk veikist, einkennamynd og magni hvítaefnisbreytinga. Fer það meðal annars eftir því hvar stökkbreytingin er staðsett í geninu. Einnig er töluverður munur á einkennum og alvarleika innan sömu fjölskyldu þó stökkbreytingin sé sú sama. Ástæðurnar fyrir þessu eru ekki fyllilega þekktar.8
Einkenni
Börn með sjúkdóminn eru yfirleitt einkennalaus, en sum geta verið með mígreni með áru frá unglingsaldri. Meðalaldur við upphaf einkenna er 30 ár og algengustu einkenni hjá fullorðnum eru mígreni með áru, TIA/heilaslag, hægt versnandi vitræn geta og geðræn einkenni.13
Mígreni með áru
Mígreni kemur fram hjá 30–75% fólks með CADASIL og byrjar oftast fyrir 30 ára aldur.14 Flestir eru með mígreni með árueinkennum (fyrirboði fyrir höfuðverkinn). Áran er yfirleitt á formi sjóntruflana, dofa, máttminnkunar eða máltruflunar.15
Stundum getur verið erfitt að meta hvort um sé að ræða mígreniáru, TIA eða vægt heilaslag. Það sem einkennir áruna er í fyrsta lagi svokölluð jákvæð einkenni (bylgjur og glampar) sem hreyfast yfir sjónsviðið. Í öðru lagi að fyrirboðaeinkennin koma ekki öll samtímis. Yfirleitt kemur sjóntruflunin fyrst, svo dofinn, máttminnkunin og loks taltruflunin hvert á fætur öðru. Ástæðan er sú að áran er afskautun (spreading depolarization) taugafrumna sem færist frá sjónberki fram á við yfir heilabörkinn. Í árunni dreifist dofinn ennfremur frá einum líkamshluta til annars. Hann byrjar til dæmis í hendi og dreifist á nokkrum mínútum upp í andlit sömu megin.
Við heilaslag koma einkennin oftast öll í einu eins og nafnið gefur til kynna.
TIA og heilaslag
Stór hluti fólks með CADASIL (60-85 prósent) fær annað hvort TIA eða heilaslag á aldrinum 18 til 67 ára (meðalaldur 51 til 53 ára).13,16,17 TIA felur í sér tímabundna blóðflæðistruflun sem veldur svipuðum einkennum og heilaslag. Einkenni hverfa innan sólarhrings og ekki sjást ummerki um skemmd með myndgreiningu.
Heilaslag er hugtak yfir blóðþurrðarslag og heilablæðingu. Í CADASIL er það venjulega blóðþurrðarslag sem á sér stað. Flest blóðþurrðarslög í CADASIL eru svokölluð smáæðardrep (lokanir á litlum slagæðum heilans). Einkenni geta falið í sér annað hvort hreinar skyntruflanir, hreinar hreyfitruflanir eða samsettar skyn- og hreyfitruflanir. Heilablæðingar koma fyrir í CADASIL en eru sjaldgæfar. Hins vegar finnast örblæðingar (microbleeds), sem sjást á segulómun (MRI), hjá 30–70 prósent fólks með sjúkdóminn.18 Þessar litlu heilablæðingar valda ekki dæmigerðum einkennum heilaslags en geta leitt til versnandi vitrænnar getu auk flogaveiki.19
Snemmkomin heilabilun
Skert vitræn geta er algeng í CADASIL. Í einni rannsókn með 176 sjúklinga (meðalaldur 51 ár) var helmingur með skerta vitræna getu.20 Um 75 prósent þróa með sér heilabilun að lokum.4 Versnandi vitsmunageta er yfirleitt nokkuð hæggeng þó að hraðari versnanir eigi sér stað, ekki síst í tengslum við heilaslag.21
Fyrstu einkennin eru gjarnan að viðkomandi verður hægari í hugsun, frumkvæði- og framtaksleysi eykst auk skertrar getu til einbeitingar og skipulagshæfni. Það hægist á flæði tals, bæði vegna erfiðleika við að finna orð og þvoglumælgi. Allt af ofannefndu leiðir til þess að félagsleg færni fer versnandi og viðkomandi missir starfshæfni.22
Geðræn einkenni
Geðræn einkenni eru nokkuð algeng og hefur verið greint frá þeim hjá rúmlega þriðjungi fólks með CADASIL, en líklega eru geðræn einkenni vangreind í sjúkdóminum.23 Þunglyndi kemur fram hjá um það bil 20 prósent. Önnur geðræn einkenni eru svefntruflanir, pirringur, kvíði, áfengisfíkn og jafnvel geðrofseinkenni. 24 Sinnuleysi, minnkaður áhugi eða skert markmiðsbundin hegðun eru algeng, ekki síst í tengslum við skerta vitræna getu.
Úttaugakvilli
Útlægur fjöltaugakvilli (polyneuropathy) getur verið síðkomið einkenni í CADASIL.4 Fjöltaugakvilli hefur áhrif á úttaugar líkamans í höndum og fótum. Algengustu einkennin eru dofi, tilfinningaleysi, óþægindi og verkir og stundum máttleysi. Verkirnir eru gjarnan verstir þegar farið er að sofa, sem getur haft áhrif á svefninn. Orsök úttaugakvilla í CADASIL er ekki fyllilega þekkt.
Flogaveiki
Flogaveiki kemur fram hjá 4-10% fólks með CADASIL.13 Bæði getur verið um staðbundin flog eða alflog að ræða. Flestir með flogaveiki hafa fengið heilaslag og oftast er það sú skemmd sem er orsök flogavirkninnar.
Sjúkdómsgangur
Sjúkdómurinn fer yfirleitt hægt versnandi. Viðvarandi skert blóðrás til heilans leiðir á endanum til frekari fötlunar, jafnvel án heilaslags. Ekki síst kemur það fram í skertri vitrænni getu, göngulagstruflunum og þvagleka.13
Greining
Grunur um CADASIL ætti að vakna hjá einstaklingi með útbreiddar, samhverfar breytingar í hvíta efni heilans án þess að hafa áhættuþætti hjarta- og æðasjúkdóma, ekki síst ef breytingarnar eru í fremri hluta gagnaugarblaðs beggja megin (temporal lobe) og gráhýði (external capsule)25 (myndir 1-3). Enn fremur ef sjúklingur eða aðstandendur hafa sögu um mígreni með áru, heilaslag eða snemmkomna vitræna skerðingu.
Hafa ber í huga að CADASIL getur verið til staðar hjá fólki með væg einkenni, jafnvel á efri árum, án sögu um heilaslag og án ættarsögu. Sumir með sjúkdóminn hafa breytingar í hvíta efni heilans þegar við tvítugsaldur og um fertugt hafa næstum allir með CADASIL ofannefndar hvítaefnisbreytingar.4 Örblæðingar (microbleeds) greinast hjá 30-70% sjúklinga með CADASIL (mynd 4).26
Hægt er að staðfesta greininguna með því að greina sjúkdómsvaldandi afbrigði NOTCH3-gensins með DNA-greiningu. Greininguna er einnig hægt að staðfesta með rannsókn á húðsýni sem inniheldur slagæðar úr húð, en með rafeindasmásjárskoðun er hægt að sjá fyrrnefndar útfellingar í vöðvafrumum slagæða (granular osmyophilic material).27 Þessi aðferð hefur þó orðið mun sjaldgæfari eftir því sem erfðarannsóknir eru auðveldari í dag. Í tengslum við greiningu er mikilvægt að bjóða upp á erfðaráðgjöf.
Helstu mismunagreiningar, bæði hvað varðar einkenni og útlit á segulómskoðun eru: MS, CARASIL (cerebral autosomal recessive arteriosclerotic arteriopathy with subcortical infarcts and leukoencephalopathy), Binswanger-sjúkdómur, ættgengt helftarmígreni, MELAS og Fabrys-sjúkdómur.28
Meðferð
Það er engin meðferð sem læknar CADASIL. Meðferðin beinist að því að draga úr og koma í veg fyrir einkenni. Þannig er mikilvægt að meðhöndla áhættuþætti hjarta- og æðasjúkdóma sem geta gert ástandið enn verra. 29
Fólk sem hefur fengið TIA eða heilablóðþurrðarslag er venjulega meðhöndlað með blóðflöguhemjandi lyfjum. Vegna hættu á blæðingum í heila er almennt ekki mælt með blóðþynnandi lyfjum til að hindra blóðþurrðarslag, nema fyrir liggi sérstakar ábendingar eins og lungnasegarek. Því þarf að meta áhættuna og ábendinguna í hverju tilfelli fyrir sig. CADASIL er hlutfallsleg (relative) frábending fyrir segaleysandi meðferð, en meta verður hvert tilfelli fyrir sig.28
Dæmi eru um að segaleysandi meðferð hafi gengið vel hjá einstaklingum með CADASIL.30 Við lokun stærri æða til heilans væri segabrottnám æskilegri meðferð en segaleysandi meðferð.
Ef um mígreniköst er að ræða er hægt að nota acetýlsalisýlsýru og parasetamól auk íbúprófens og annarra COX-hemla. Meðferð með æðaherpandi lyfjum eins og triptönum (triptans) kemur til greina og er ekki sami fyrirvari settur við þá meðferð eins og áður var hjá CADASIL-sjúklingum.1,31 Viss efi hefur verið um notkun með CGRP-hemlum (calcitonin gene related peptide inhibitors) þar sem þeir koma í veg fyrir æðaútvíkkun og áhrifin á CADASIL eru enn óþekkt. Þó hafa verið birtar einstaka tilfellarannsóknir þar sem þetta hefur gengið vel.32
Ef mígreniköstin eru tíð, þrisvar í mánuði eða oftar, geta fyrirbyggjandi lyf verið nauðsynleg. Vissar vísbendingar hafa verið uppi um að ósértækir beta-blokkar séu ekki æskilegir sem fyrirbyggjandi meðferð við mígreni hjá fólki með CADASIL.31
Við meðhöndlun geðrænna einkenna skal fylgja almennum leiðbeiningum um meðferð geðsjúkdóma. Flogaveiki er meðhöndluð á hefðbundinn hátt með flogalyfjum. Gæta skal varúðar við að nota getnaðarvörn sem inniheldur estrógen í ljósi aukinnar hættu á blóðtappa. Á meðgöngu eru konur með sjúkdóminn í aukinni hættu á meðgöngueitrun og því er sérhæfð mæðravernd mikilvæg.33
Oft er þörf á endurhæfingu til að endurheimta og viðhalda eins góðri heilsu og mögulegt er. Þetta felur í sér þjálfun í hreyfifærni, tali og vitrænni starfsemi. Fer það eftir umfangi fötlunar hvaða aðstoð hver og einn þarf. Að lifa með síversnandi sjúkdóm getur verið mikið álag bæði fyrir einstaklinginn og fjölskylduna. Því er mikilvægt að þörfinni fyrir félagslegan og sálrænan stuðning sé mætt. Eftir því sem sjúkdómurinn ágerist, vex þörfin fyrir aðstoð og stuðning í daglegu lífi.
Færð hafa verið ágætis rök fyrir því að þýski heimspekingurinn Friedrich Nietzsche (1844-1900) hafi veikst af CADASIL frekar en sárasótt eins og áður var talið.34,35
Á fyrri hluta æviskeiðsins þjáðist Nietzsche af erfiðum höfuðverkjaköstum sem að öllum líkindum voru mígreniköst. Sagði hann upp stöðu sinni sem prófessor í Basel vegna þessa og gerðist landflótta í leit að veðurfari sem hentaði heilsu hans. Síðar á ævinni fór að bera á geðrænum einkennum sem leiddu að lokum til taugaáfalls 1888. Í kjölfarið komu fram einkenni heilabilunar og loks heilaslag undir lok ævi hans. Þess ber að geta að faðir Nietzsche lést einnig fyrir aldur fram vegna áþekkra einkenna.
Samantekt
CADASIL er sjaldgæfur arfgengur smáæðasjúkdómur í heila þar sem orsökin er sjúkdómsvaldandi stökkbreyting í NOTCH3--geninu á 19. litningi. Gallað prótein safnast fyrir á yfirborði sléttra vöðvafrumna í litlum slagæðum heilans. Fyrir vikið verða æðarnar stífari og þrengri og geta til æðavíkkunar skerðist. Mígreni með áru, skammvinn heilablóðþurrð eða heilaslag, auk geðrænna einkenna og snemmkominnar heilabilunar eru helstu afleiðingar sjúkdómsins.
CADASIL er mikilvæg orsök heilaslags og snemmkominnar heilabilunar hjá ungu og miðaldra fólki og líklega vangreint. Engin sértæk meðferð er til við sjúkdóminum en mikilvægt er að meðhöndla brátt heilaslag og aðra áhættuþætti hjarta- og æðasjúkdóma með hefðbundnum hætti auk meðferðar við mígreni, flogaveiki, geðrænum einkennum og heilabilun. Í tengslum við greiningu er mikilvægt að bjóða upp á erfðaráðgjöf.
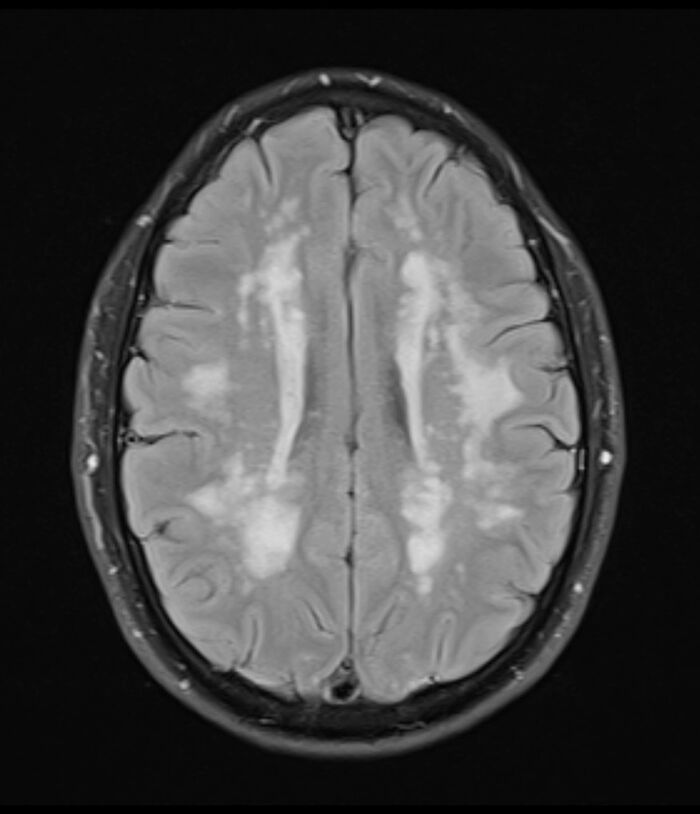
Mynd 1. FLAIR (Fluid Attenuated Inversion Recovery) segulómun hjá sjúklingi með CADASIL, sem sýnir útbreiddar samfelldar segulskærar hvítaefnisbreytingar í báðum heilahvelum.
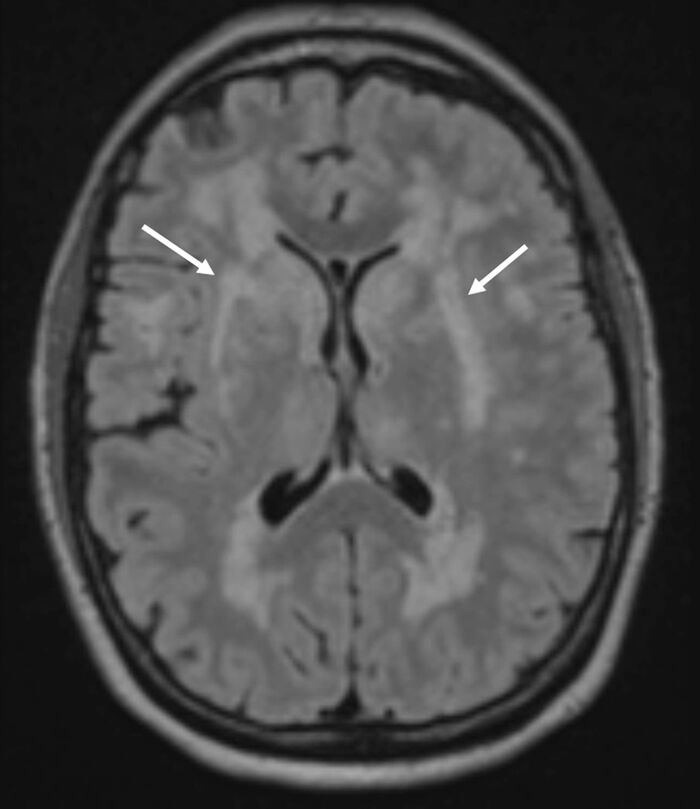
Mynd 2. FLAIR-mynd hjá sjúklingi með CADASIL, sem sýnir dæmigerðar segulskærar hvítaefnisbreytingar, meðal annars í gráhýði (external capsule) beggja vegna (hvítar örvar).
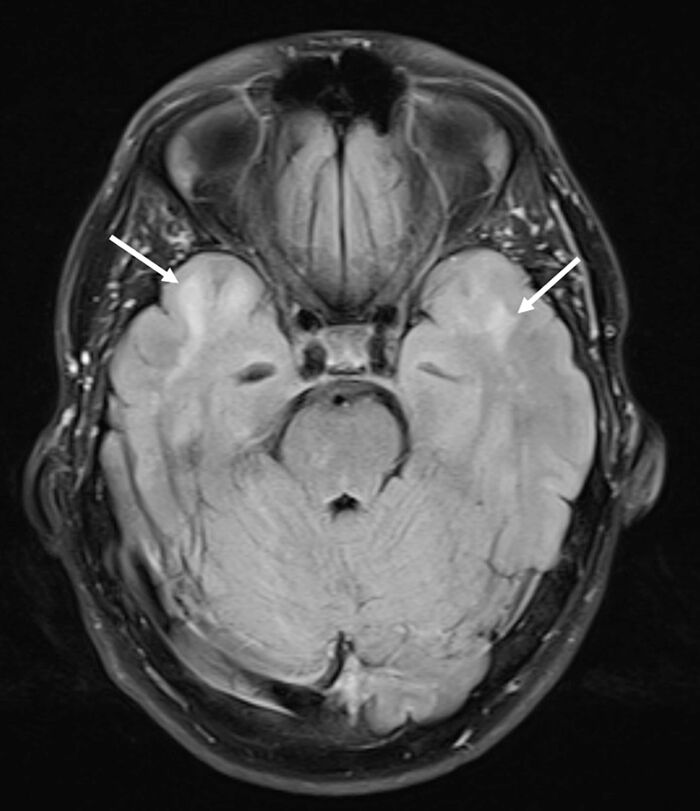
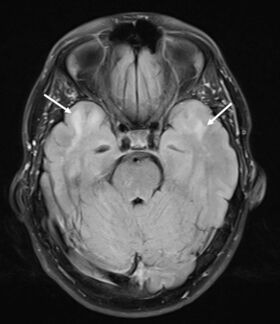
Mynd 3. FLAIR-mynd hjá sama sjúklingi með CADASIL, sem sýnir dæmigerðar segulskærar hvítaefnisbreytingar í fremri hluta beggja gagnaugarblaða (hvítar örvar).
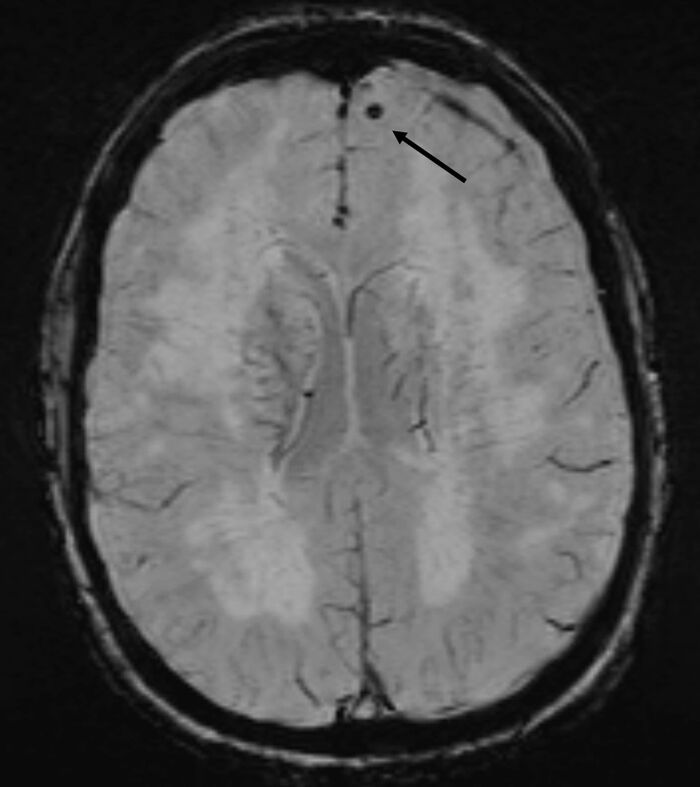
Mynd 4. SWI (Susceptibility Weighted Imaging) segulómun sem sýnir eina örblæðingu fremst í vinstra ennisblaði (svört ör).
Heimildir
| 1. Mancuso M, Arnold M, Bersano A, et al. Monogenic cerebral small-vessel diseases: diagnosis and therapy. Consensus recommendations of the European Academy of Neurology. Euro J of Neurology 2020;27(6):909-27. https://doi.org/10.1111/ene.14183 PMid:32196841 |
||||
| 2. van Bogaert L. Encéphalopathie sous-corticale progressive (Binswanger) a evolution rapide chez deux soeurs. Med Hellen 1955;24:961-72. | ||||
| 3. Sonninen V, Savontaus ML. Hereditary Multi-Infarct Dementia. Eur Neurol 1987;27(4):209-15. https://doi.org/10.1159/000116158 PMid:3678285 |
||||
| 4. Chabriat H, Joutel A, Dichgans M, et al. CADASIL. The Lancet Neurology 2009;8(7):643-53. https://doi.org/10.1016/S1474-4422(09)70127-9 PMid:19539236 |
||||
| 5. Domenga V, Fardoux P, Lacombe P, et al. Notch3 is required for arterial identity and maturation of vascular smooth muscle cells. Genes Dev 2004;18(22):2730-5. https://doi.org/10.1101/gad.308904 PMid:15545631 PMCid:PMC528893 |
||||
| 6. Razvi SSM. The prevalence of cerebral autosomal dominant arteriopathy with subcortical infarcts and leucoencephalopathy (CADASIL) in the west of Scotland. JNNP 2005;76(5):739-41. https://doi.org/10.1136/jnnp.2004.051847 PMid:15834040 PMCid:PMC1739620 |
||||
| 7. Cho BPH, Nannoni S, Harshfield EL, et al. NOTCH3 variants are more common than expected in the general population and associated with stroke and vascular dementia: an analysis of 200 000 participants. J Neurol Neurosurg Psychiatry 2021;92(7):694-701. https://doi.org/10.1136/jnnp-2020-325838 PMid:33712516 PMCid:PMC8223663 |
||||
| 8. Rutten JW, Hack RJ, Duering M, et al. Broad phenotype of cysteine-altering NOTCH3 variants in UK Biobank: CADASIL to nonpenetrance. Neurology 2020;95(13):e1835-43. https://doi.org/10.1212/WNL.0000000000010525 PMid:32732295 PMCid:PMC7682826 |
||||
| 9. High FA, Zhang M, Proweller A, et al. An essential role for Notch in neural crest during cardiovascular development and smooth muscle differentiation. J Clin Invest 2007;117(2):353-63. https://doi.org/10.1172/JCI30070 PMid:17273555 PMCid:PMC1783803 |
||||
| 10. Malka K, Liaw L. NOTCH3 as a modulator of vascular disease: a target in elastin deficiency and arterial pathologies. J Clin Invest 2022;132(5):e157007. https://doi.org/10.1172/JCI157007 PMid:35229725 PMCid:PMC8884893 |
||||
| 11. Monet-Leprêtre M, Haddad I, Baron-Menguy C, et al. Abnormal recruitment of extracellular matrix proteins by excess Notch3ECD: a new pathomechanism in CADASIL. Brain 2013;136(6):1830-45. https://doi.org/10.1093/brain/awt092 PMid:23649698 PMCid:PMC3673461 |
||||
| 12. Cramer J, White ML. Cerebral Autosomal Dominant Arteriopathy. Treasure Island (FL): StatPearls; 2024. | ||||
| 13. Dichgans M, Mayer M, Uttner I, et al. The phenotypic spectrum of CADASIL: Clinical findings in 102 cases. Ann Neurol 1998;44(5):731-9. https://doi.org/10.1002/ana.410440506 PMid:9818928 |
||||
| 14. Liem MK, Oberstein SAL, Van Der Grond J, et al. CADASIL and migraine: A narrative review. Cephalalgia 2010;30(11):1284-9. https://doi.org/10.1177/0333102410370870 PMid:21038489 |
||||
| 15. Guey S, Mawet J, Hervé D, et al. Prevalence and characteristics of migraine in CADASIL. Cephalalgia 2016;36(11):1038-47. https://doi.org/10.1177/0333102415620909 PMid:26646784 |
||||
| 16. Ling Y, De Guio F, Duering M, et al. Predictors and Clinical Impact of Incident Lacunes in Cerebral Autosomal Dominant Arteriopathy With Subcortical Infarcts and Leukoencephalopathy. Stroke 2017;48(2):283-9. https://doi.org/10.1161/STROKEAHA.116.015750 PMid:28034964 |
||||
| 17. Opherk C. Long-term prognosis and causes of death in CADASIL: a retrospective study in 411 patients. Brain 2004;127(11):2533-9. https://doi.org/10.1093/brain/awh282 PMid:15364702 |
||||
| 18. Rinnoci V, Nannucci S, Valenti R, et al. Cerebral hemorrhages in CADASIL: Report of four cases and a brief review. J Neurol Sci 2013;330(1-2):45-51. https://doi.org/10.1016/j.jns.2013.04.002 PMid:23639391 |
||||
| 19. Anamnart C, Songsaeng D, Chanprasert S. A large number of cerebral microbleeds in CADASIL patients presenting with recurrent seizures: a case report. BMC Neurol 2019;19(1):106. https://doi.org/10.1186/s12883-019-1342-2 PMid:31146726 PMCid:PMC6542033 |
||||
| 20. Jolly AA, Nannoni S, Edwards H, et al. Prevalence and Predictors of Vascular Cognitive Impairment in Patients With CADASIL. Neurology 2022;99(5). https://doi.org/10.1212/WNL.0000000000200607 |
||||
| 21. Amberla K, Wäljas M, Tuominen S, et al. Insidious Cognitive Decline in CADASIL. Stroke 2004;35(7):1598-602. https://doi.org/10.1161/01.STR.0000129787.92085.0a PMid:15143298 |
||||
| 22. Peters N, Opherk C, Danek A, et al. The Pattern of Cognitive Performance in CADASIL: A Monogenic Condition Leading to Subcortical Ischemic Vascular Dementia. AJP 2005;162(11):2078-85. https://doi.org/10.1176/appi.ajp.162.11.2078 PMid:16263847 |
||||
| 23. Leyhe T, Wiendl H, Buchkremer G, et al. CADASIL: underdiagnosed in psychiatric patients? Acta Psychiatr Scand 2005;111(5):392-6. https://doi.org/10.1111/j.1600-0447.2004.00452.x PMid:15819734 |
||||
| 24. Valenti R, Poggesi A, Pescini F, et al. Psychiatric disturbances in CADASIL: a brief review. Acta Neurol Scand 2008;118(5):291-5. https://doi.org/10.1111/j.1600-0404.2008.01015.x PMid:18384453 |
||||
| 25. Auer DP, Pütz B, Gössl C, et al. Differential Lesion Patterns in CADASIL and Sporadic Subcortical Arteriosclerotic Encephalopathy: MR Imaging Study with Statistical Parametric Group Comparison. Radiology 2001;218(2):443-51. https://doi.org/10.1148/radiology.218.2.r01fe24443 PMid:11161160 |
||||
| 26. Viswanathan A, Chabriat H. Cerebral Microhemorrhage. Stroke 2006;37(2):550-5. https://doi.org/10.1161/01.STR.0000199847.96188.12 PMid:16397165 |
||||
| 27. Smith BW, Henneberry J, Connolly T. Skin biopsy findings in CADASIL. Neurology 2002;59(6):961-961. https://doi.org/10.1212/WNL.59.6.961 PMid:12297597 |
||||
| 28. Meschia JF, Worrall BB, Elahi FM, et al. Management of Inherited CNS Small Vessel Diseases: The CADASIL Example: A Scientific Statement From the American Heart Association. Stroke 2023;54(10). https://doi.org/10.1161/STR.0000000000000444 |
||||
| 29. Adib-Samii P, Brice G, Martin RJ, et al. Clinical Spectrum of CADASIL and the Effect of Cardiovascular Risk Factors on Phenotype: Study in 200 Consecutively Recruited Individuals. Stroke 2010;41(4):630-4. https://doi.org/10.1161/STROKEAHA.109.568402 PMid:20167921 |
||||
| 30. Pescini F, Torricelli S, Squitieri M, et al. Intravenous thrombolysis in CADASIL: report of two cases and a systematic review. Neurol Sci 2023;44(2):491-8. https://doi.org/10.1007/s10072-022-06449-2 PMid:36255541 PMCid:PMC9842556 |
||||
| 31. Glover PA, Goldstein ED, Badi MK, et al. Treatment of migraine in patients with CADASIL: A systematic review and meta-analysis. Neur Clin Pract 2020;10(6):488-96. https://doi.org/10.1212/CPJ.0000000000000769 PMid:33520412 PMCid:PMC7837435 |
||||
| 32. Albanese M, Pescini F, Di Bonaventura C, et al. Long-Term Treatment with the Calcitonin Gene-Related Peptide Receptor Antagonist Erenumab in CADASIL: Two Case Reports. JCM 2024;13(7):1870. https://doi.org/10.3390/jcm13071870 PMid:38610637 PMCid:PMC11012730 |
||||
| 33. Roine S, Pöyhönen M, Timonen S, et al. Neurologic symptoms are common during gestation and puerperium in CADASIL. Neurology 2005;64(8):1441-3. https://doi.org/10.1212/01.WNL.0000158655.71323.8A PMid:15851739 |
||||
| 34. Hemelsoet D, Hemelsoet K, Devreese D. The neurological illness of Friedrich Nietzsche. Acta Neurol Belg 2008;108(1):9-16. | ||||
| 35. Perogamvros L, Perrig S, Bogousslavsky J, et al. Friedrich Nietzsche and his Illness: A Neurophilosophical Approach to Introspection. J Hist Neurosci 2013;22(2):174-82. https://doi.org/10.1080/0964704X.2012.712825 PMid:23586545 |
||||